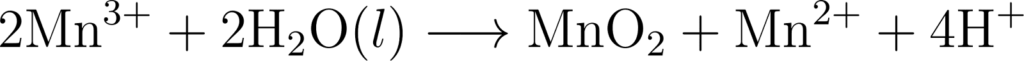रसायनशास्त्र एक बहुत ही कठिन विषय है खासकर इसमे दिय गय रासायनिक समीकरण इस विषय को और भी कठिन बना देते हैं। यहाँ हमने एनसीईआरटी कक्षा 11 रसायनशास्त्र अध्याय 08 अपचयोपचय अभिक्रियाएँ समाधान दिया हैं। बोर्डस्टडि द्वारा दिया गया कक्षा 11 रसायनशास्त्र समाधान एनसीईआरटी पुस्तक के अनुसार तैयार किए गए हैं।
यह समाधान छात्रो मे आत्मविश्वास लाने का काम करेगा एवं परीक्षा मे अच्छा स्कोर करने मे मदद करेगा। इस अध्याय की मदद से आप ऑक्सीकरण और अपचयन, ऑक्सीकरण संख्या, रेडॉक्स अभिक्रियाओं के प्रकार, तथा संतुलन की विधियाँ जैसी मूलभूत धारणाओ से जुड़ी सभी प्रश्न और उत्तर को अच्छे से समझ सकते हैं। समाधान मे सभी आवधारनाओ को सरल एवं आसान भाषा मे समझाया गया हैं।
अपचयोपचय अभिक्रियाएँ संरचना समाधान

































अध्याय 07 : कार्बनिक रसायन – कुछ आधारभूत सिद्धान्त तथा तकनीकें संरचना
अध्याय 09 : हाइड्रोकार्बन
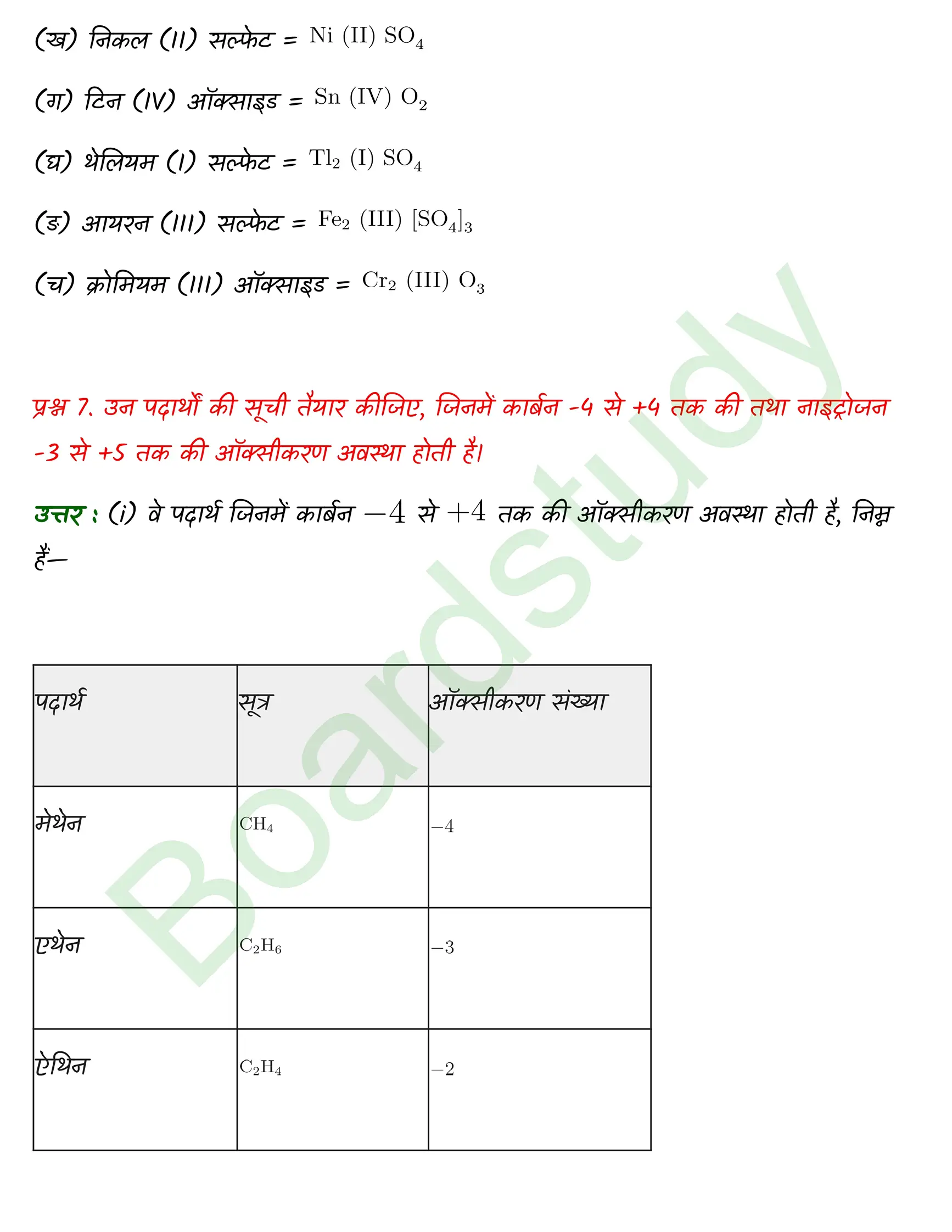
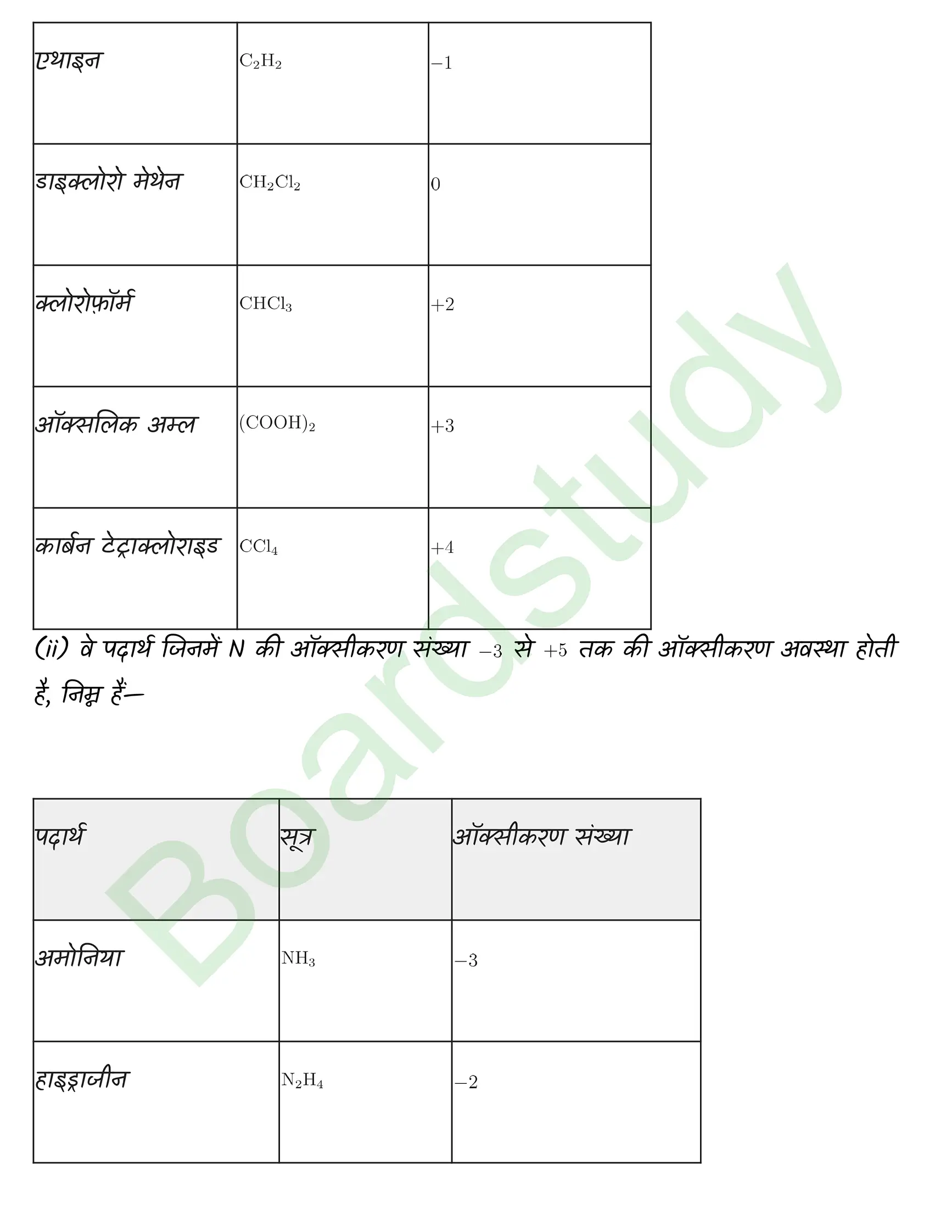
एनसीईआरटी अध्याय 08 अपचयोपचय अभिक्रियाएँ के महत्वपूर्ण प्रश्न
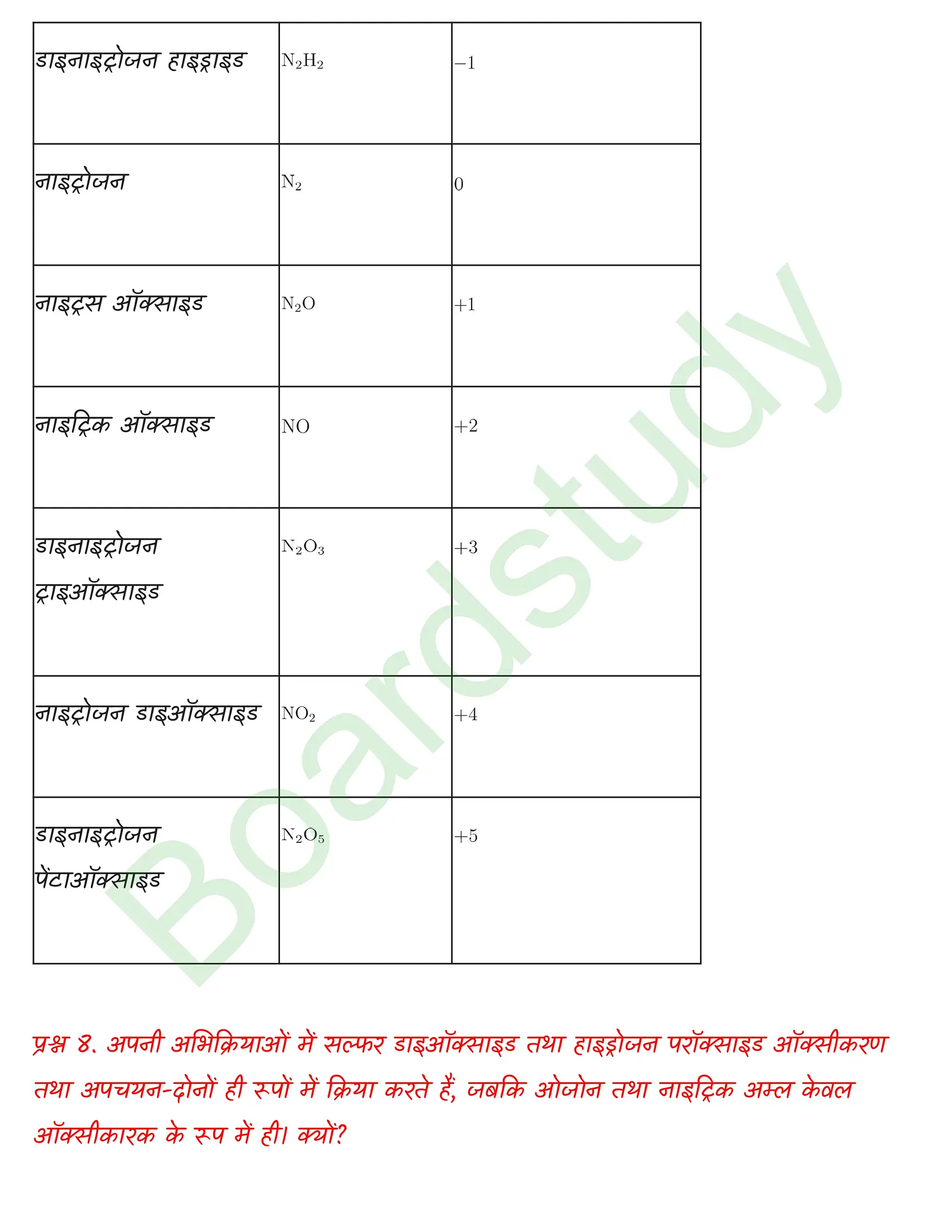
प्रश्न. अपनी अभिक्रियाओं में सल्फर डाइऑक्साइड तथा हाइड्रोजन परॉक्साइड ऑक्सीकरण तथा अपचयन-दोनों ही रूपों में क्रिया करते हैं, जबकि ओजोन तथा नाइट्रिक अम्ल केवल ऑक्सीकारक के रूप में ही। क्यों?
उत्तर : हाइड्रोजन परॉक्साइड (H2O2) एवं सल्फर डाइऑक्साइड (SO2) में S तथा O की ऑक्सीकारक संख्या बढ़ या घट सकती है; अतः दोनों ऑक्सीकारक एवं अपचायक के रूप में होते हैं। ओजोन में ऑक्सीजन की ऑक्सीकारक संख्या केवल घटती है। अतः यह ऑक्सीकारक के रूप में होता है। इसी प्रकार, नाइट्रोजन की अधिकतम ऑक्सीकारक अवस्था +5 है, जो केवल घट सकती है; अतः यह ऑक्सीकारक के रूप में होता है।
प्रश्न 21. Mn3+ आयन विलयन में अस्थायी होता है तथा असमानुपात द्वारा M2+ , MnO2 और H+ आयन देता है। इस अभिक्रिया के लिए सन्तुलित आयनिक समीकरण लिखिए।
उत्तर : अभिक्रिया :
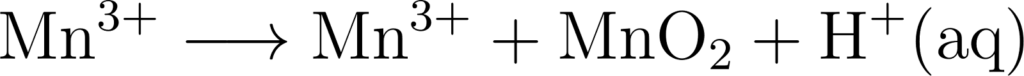
अर्द्ध ऑक्सीकारक अभिक्रिया :
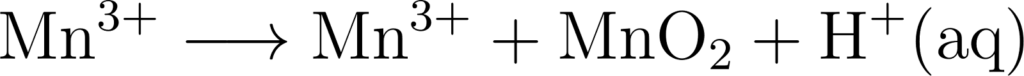
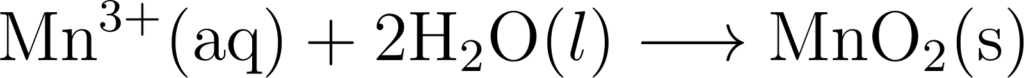

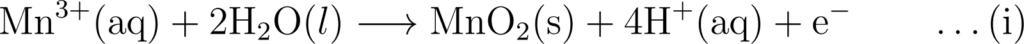
अर्द्ध अपचयन अभिक्रिया :
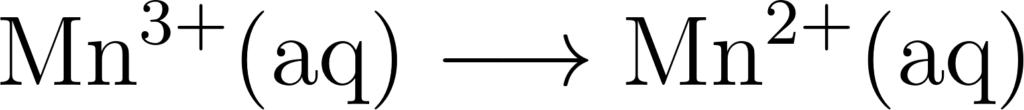
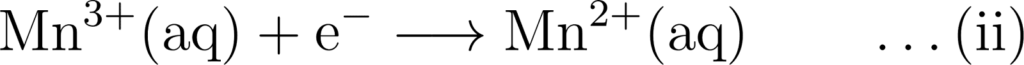
समीकरण (i) एवं (ii) को जोड़ने पर,