रसायनशास्त्र एक बहुत ही कठिन विषय है खासकर इसमे दिय गय रासायनिक समीकरण इस विषय को और भी कठिन बना देते हैं। यहाँ हमने एनसीईआरटी कक्षा 11 रसायनशास्त्र अध्याय 03 तत्वों का वर्गीकरण समाधान दिया हैं। बोर्डस्टडि द्वारा दिया गया कक्षा 11 रसायनशास्त्र समाधान एनसीईआरटी पुस्तक के अनुसार तैयार किए गए हैं।
यह समाधान छात्रो मे आत्मविश्वास लाने का काम करेगा एवं परीक्षा मे अच्छा स्कोर करने मे मदद करेगा। इस अध्याय की मदद से आप तत्वों का आवर्त वर्गीकरण, आवर्त सारणी, समूह एवं आवर्त, तथा तत्वों के गुणों में आवर्तिता जैसी मूलभूत धारणाओ से जुड़ी सभी प्रश्न और उत्तर को अच्छे से समझ सकते हैं। समाधान मे सभी आवधारनाओ को सरल एवं आसान भाषा मे समझाया गया हैं।
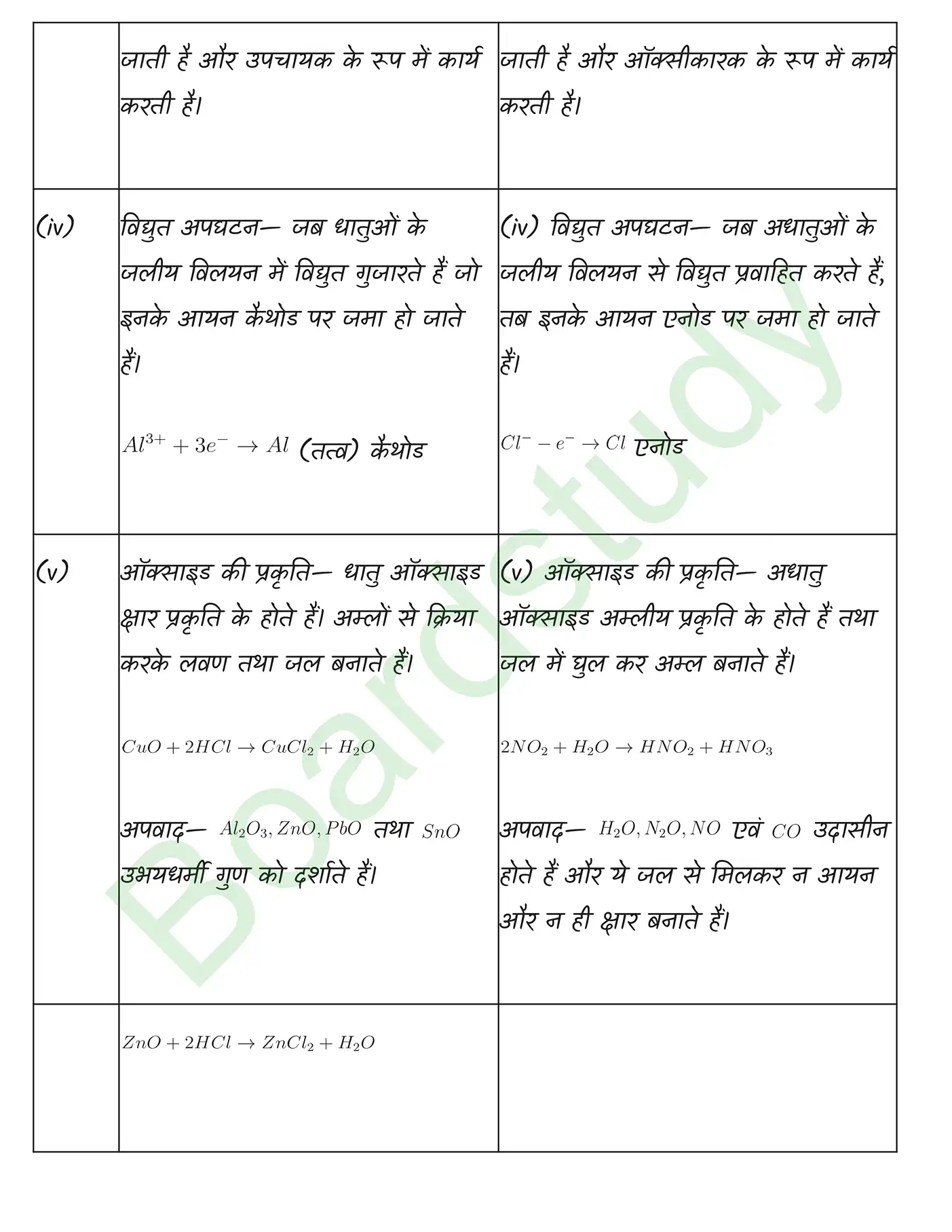
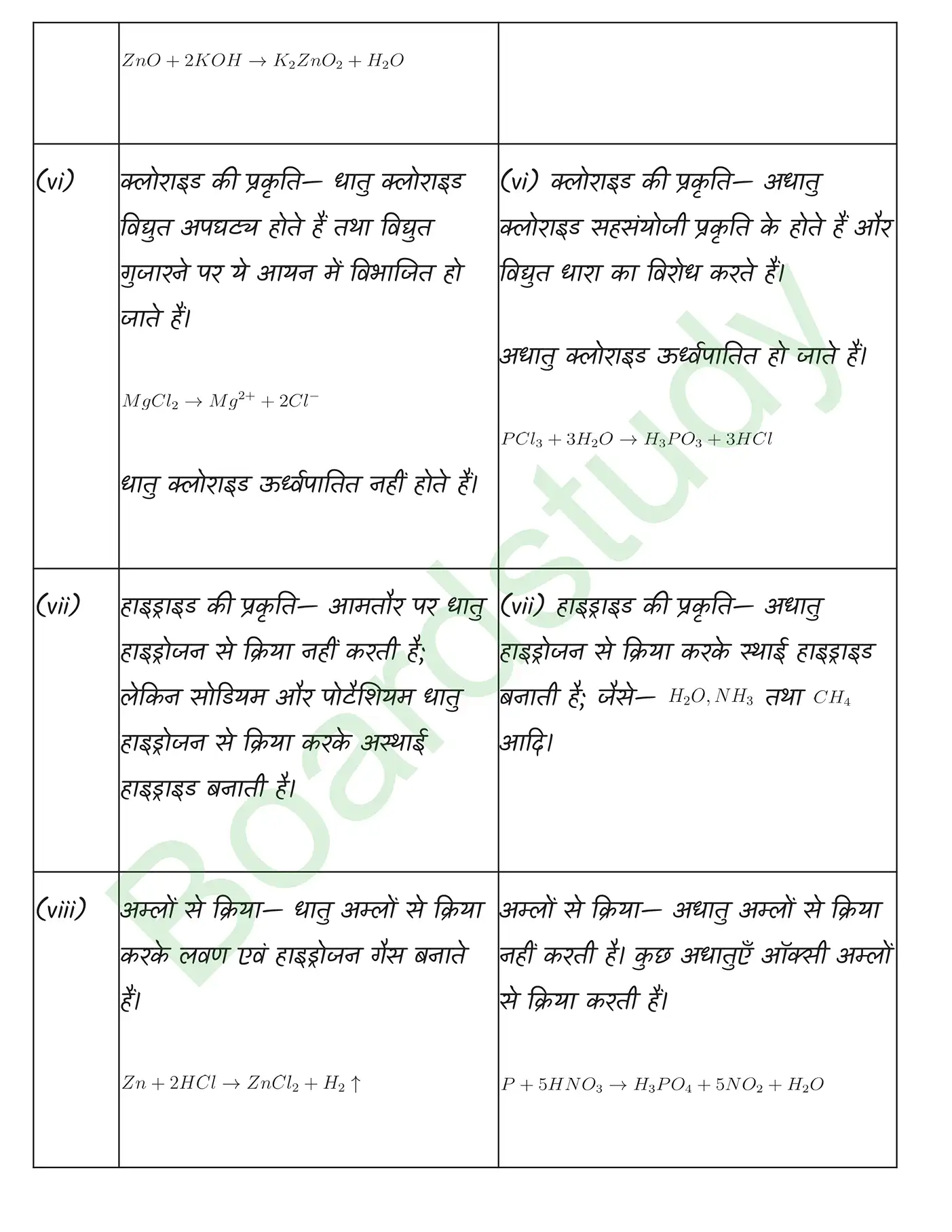
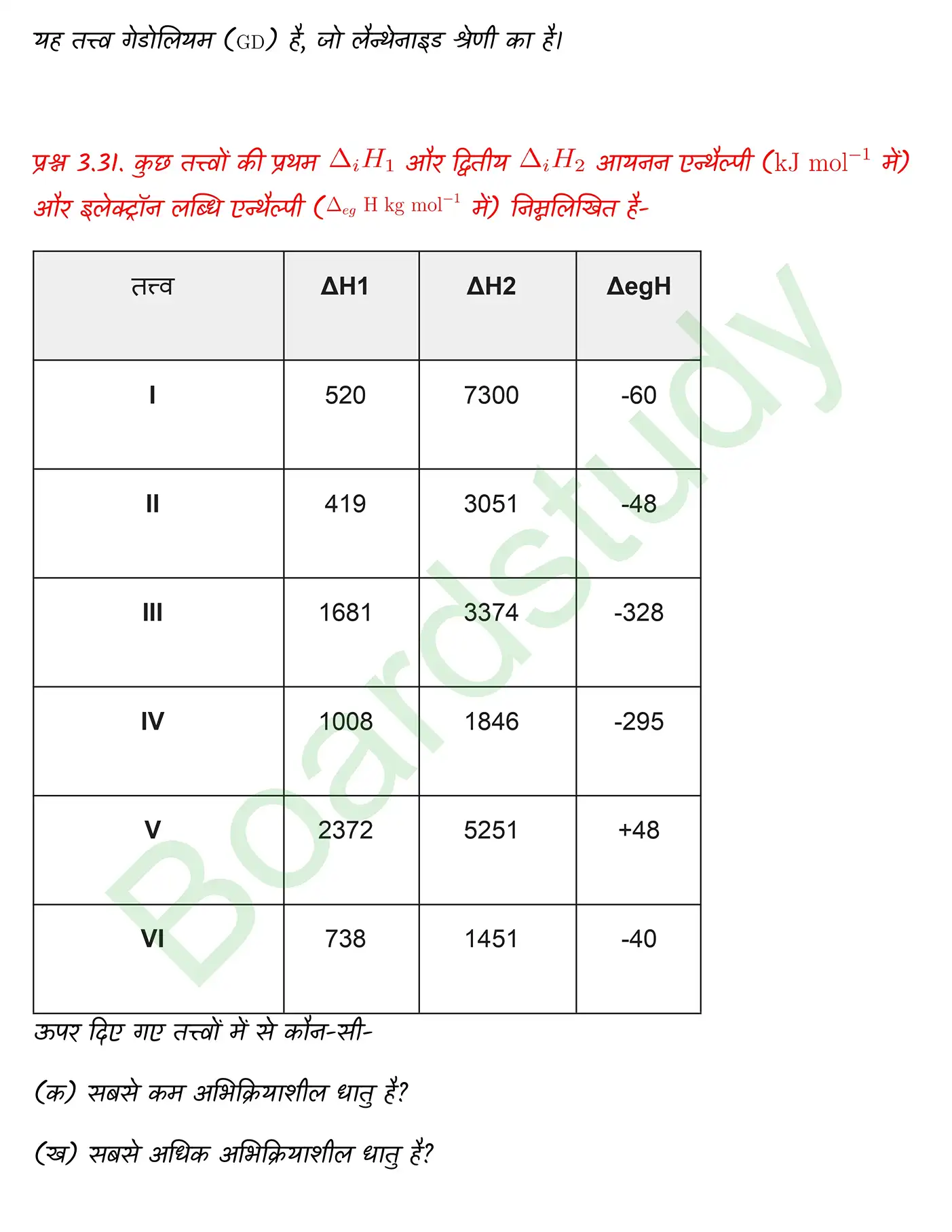
तत्वों का वर्गीकरण समाधान













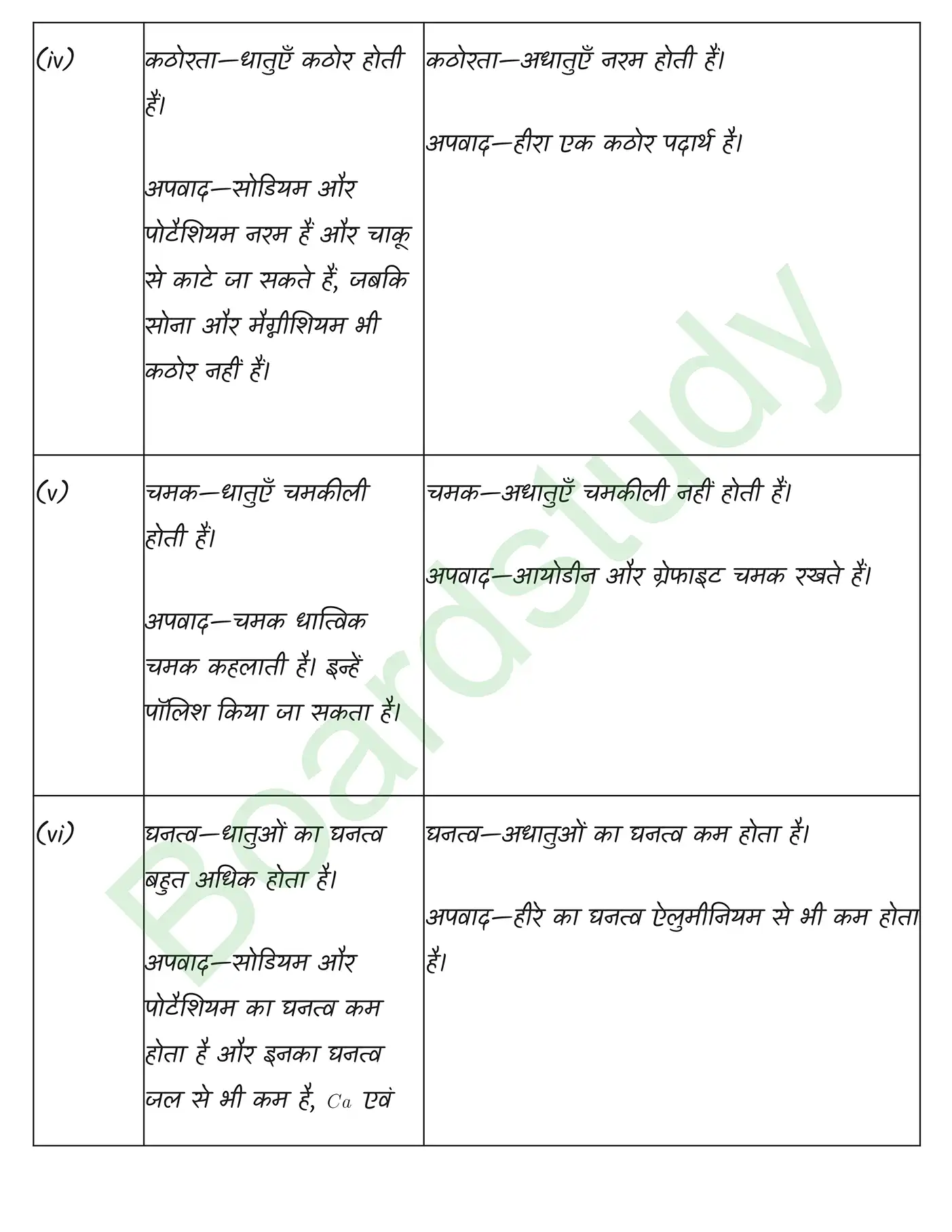
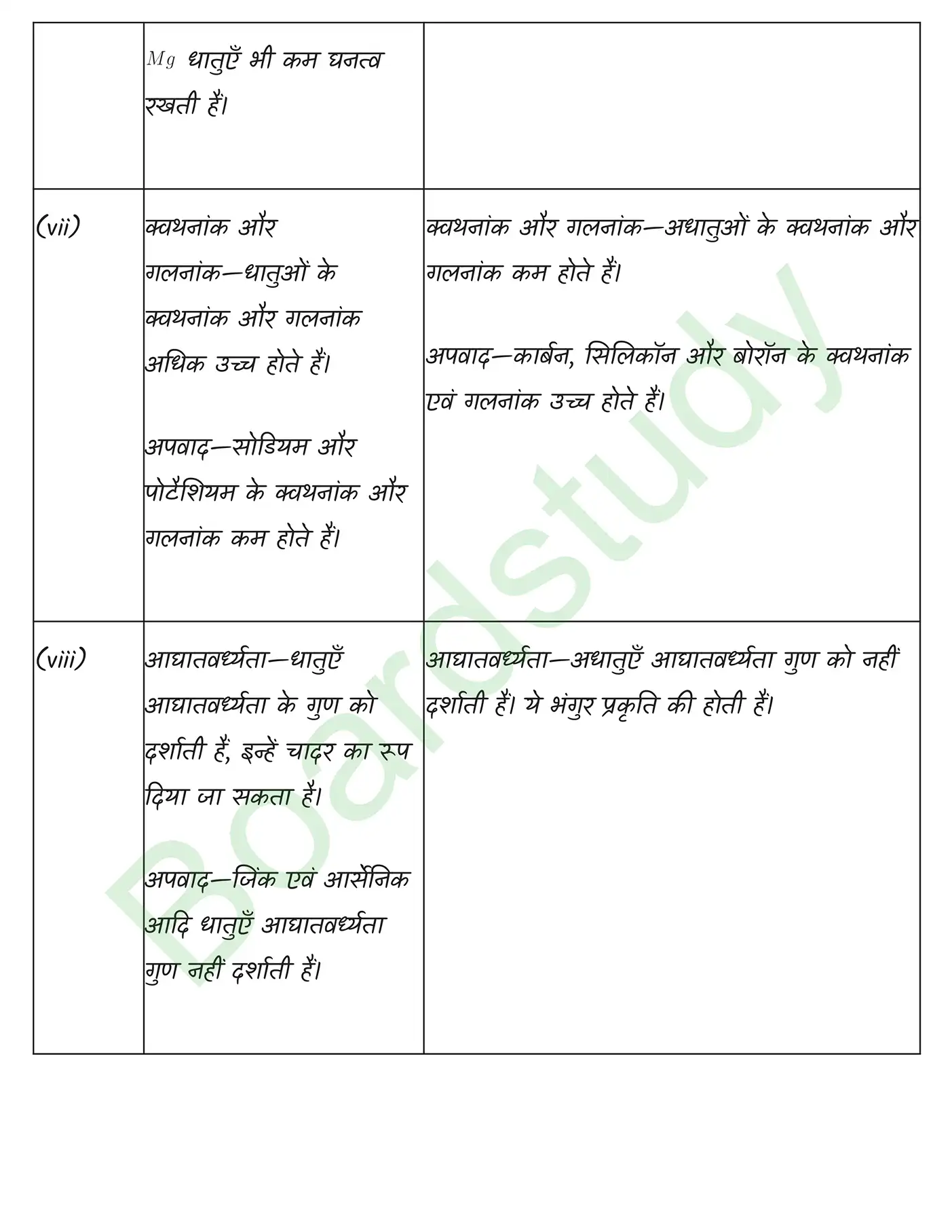
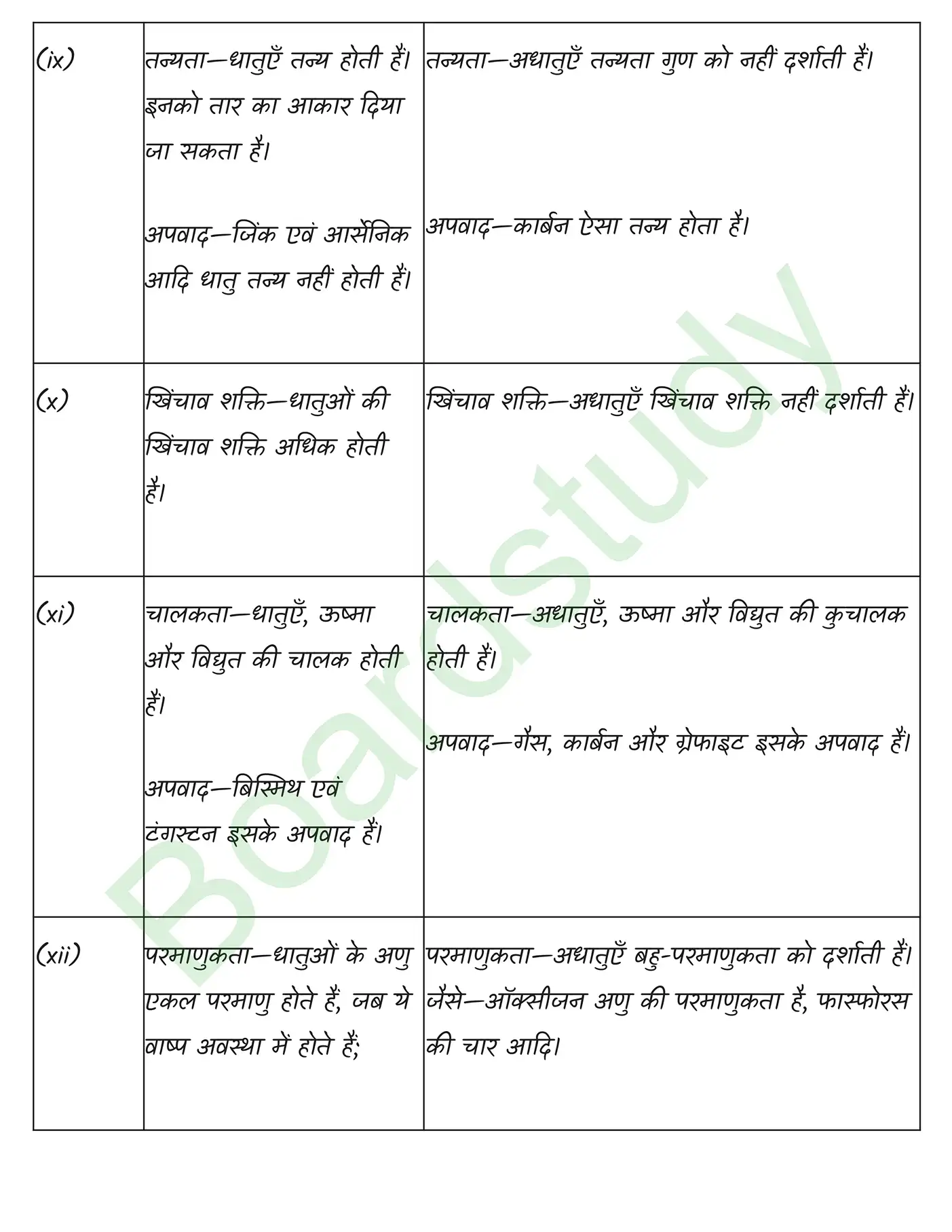
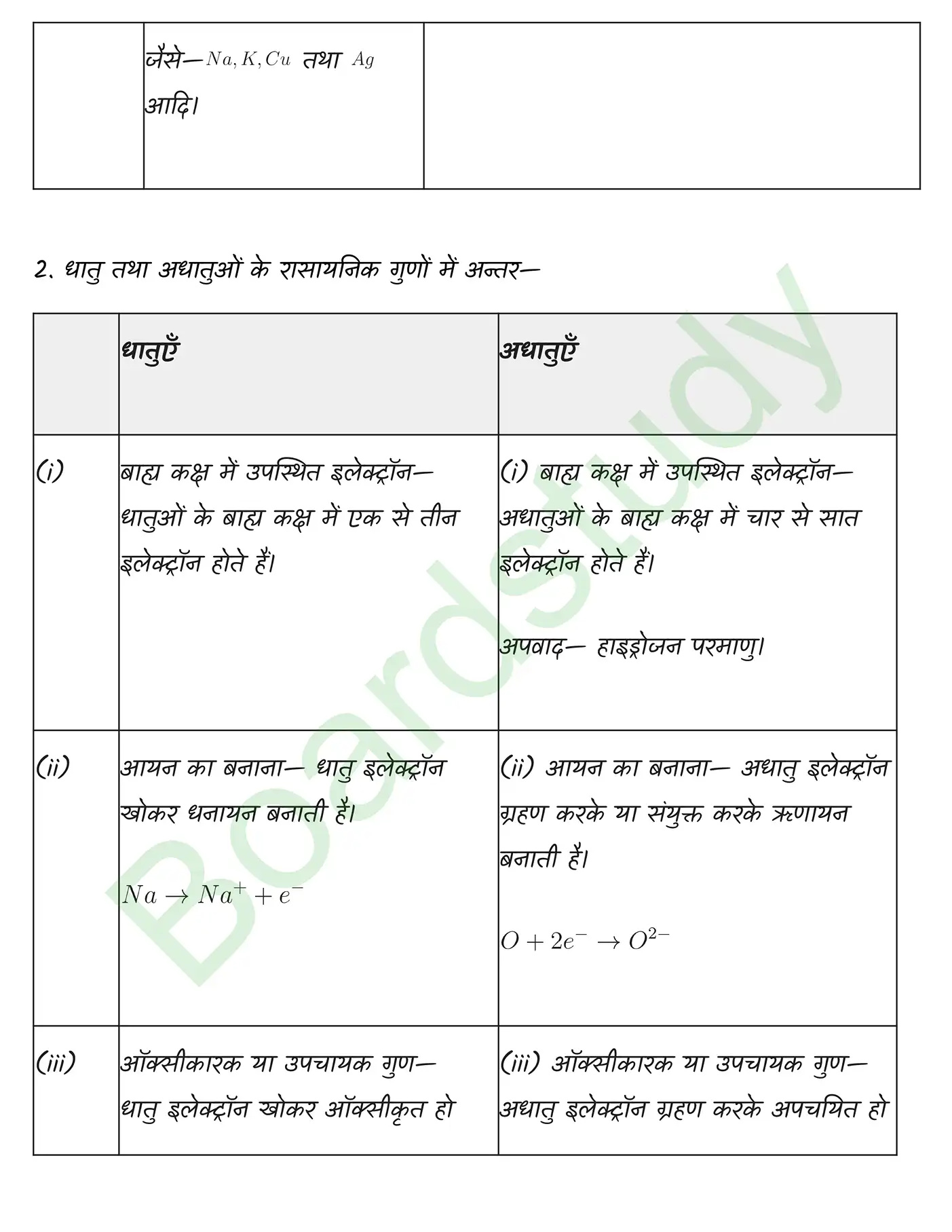








अध्याय 02 : परमाणु संरचना
अध्याय 04 : रासायनिक आबंधन तथा आण्विक संरचना
एनसीईआरटी अध्याय 03 तत्वों का वर्गीकरण के महत्वपूर्ण प्रश्न
प्रश्न. हाइड्रोजन परमाणु में आद्य अवस्था में इलेक्ट्रॉन की ऊर्जा है। परमाण्विक हाइड्रोजन की आयनन एन्थैल्पी के पदों में परिकलित कीजिए।
उत्तर : आद्य अवस्था में इलेक्ट्रॉन की ऊर्जा
इलेक्ट्रॉन मुक्त करने में ऊर्जा की आवश्यकता
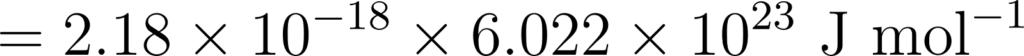
मोल संकल्पना अनुसार,
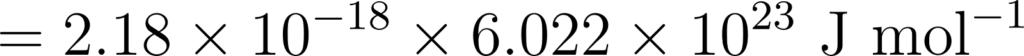
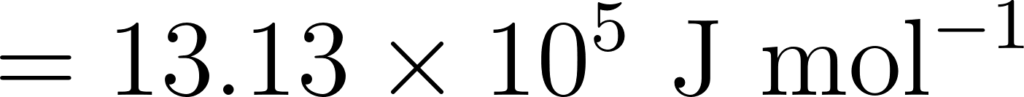
प्रश्न. मुख्य समूह तत्त्वों में आयनन एन्थैल्पी के किसी समूह में नीचे की ओर कम होने के कारक कौन-से हैं?
उत्तर : (i) नाभिकीय आवेश वर्ग के नीचे की ओर जाते समय बढ़ता है, जिसके कारण आकर्षण बल बढ़ता है और आयनन ऊर्जा का मान बढ़ता है।
(ii) नया कक्ष बढ़ने से इलेक्ट्रॉन की संख्या बढ़ती है, जिसके कारण आवरण प्रभाव या परिरक्षण प्रभाव बढ़ता है। आवरण प्रभाव के बढ़ने से इलेक्ट्रॉन और नाभिक के मध्य आकर्षण बल बढ़ता है। इसके कारण आयनन एन्थैल्पी घटती है।
(iii) वर्ग में नीचे की ओर जाते समय परमाणु आकार बढ़ता है; क्योंकि प्रत्येक परमाणु में एक नया कक्ष जुड़ता चला जाता है, जिसके कारण बाह्य इलेक्ट्रॉन और नाभिक के बीच दूरी बढ़ती है और आकर्षण बल कम हो जाता है। अतः आयनन एन्थैल्पी घटती है।
नाभिक आवेश से परमाणु आकार और आवरण प्रभाव तुलनात्मक रूप से अधिक सक्रिय है। अतः इलेक्ट्रॉन आसानी से दूर किया जा सकता है।