इस पोस्ट मे हमने एनसीईआरटी के नवीनतम पाठ्यक्रम के अनुसार कक्षा 12 रसायनशास्त्र अध्याय 2 वैधुतरसायन का समाधान दिया हैं। हमने अध्याय मे मौजूद सभी प्रश्नों का समाधान सरल एवं स्पष्ट भाषा मे दिया हैं।
छात्रो के लिय वैधुतरसायन अध्याय को अच्छे से समझना बहुत जरूरी हैं। इस अध्याय की मदद से ऑक्सीकरण-अपचयन (Redox) अभिक्रियाओं, इलेक्ट्रोड विभव, बैटरी, ईंधन सेल, और विद्युत अपघटन (electrolysis) पर आधारित है, जहाँ रासायनिक ऊर्जा को बिजली स्तर जैसी मूलभूत धारणाओ को अच्छे से समझ सकते हैं। परीक्षा मे अच्छा स्कोर करने के लिय इन धारणाओ को अच्छे से समझना बहुत जरूरी हैं।
वैधुतरसायन समाधान


























अध्याय 1: विलयन समाधान
अध्याय 3: रसायनिक बलगतिकी समाधान
अध्याय को अच्छे से समझने के लिय अध्याय मे दिय गय सभी प्रश्नों एवं अतिरिक्त प्रश्नों का अभ्यास बहुत जरूरी हैं। पिछले वर्ष का प्रश्न पत्र हल करना भी एक्जाम की तैयारी मे काफी मददगार साबित होता हैं।
एनसीईआरटी कक्षा 12 रसायनशास्त्र अध्याय 2 वैधुतरसायन के महत्वपूर्ण प्रश्न
Q. समझाइए कि कैसे लोहे पर जंग लगने का कारण एक वैद्युतरासायनिक सेल बनना माना जाता है?
उत्तर: संक्षारण में, धातु अपने इलेक्ट्रॉनों को ऑक्सीजन देकर ऑक्सीकृत होती है तथा ऑक्साइड बनाती है। जिसके कारण एक वैद्युत रासायनिक सेल स्थापित हो जाता है। उदाहरण लोहे पर जंग लगने में निम्नलिखित क्रियाएँ होती है।
(i) लोहे की सतह पर उपस्थित जल की परत वायु जैसे में घुलकर अम्लीय ऑक्साइड बनाती है। तथा बने अम्ल उत्पन्न करते हैं।
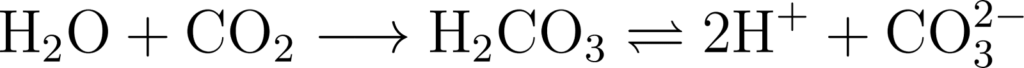
(ii) H+ आयनों की उपस्थिति में, लोहा कुछ स्थानों पर इलेक्ट्रॉनों का त्याग करके फेरस आयन बनाना प्रारम्भ कर देता है। ये स्थान ऐनोड का कार्य करते हैं।
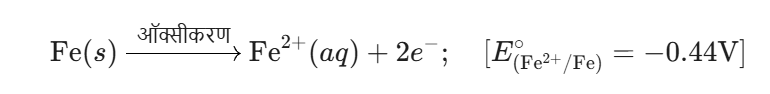
(iii) ऐनोड पर मुक्त इलेक्ट्रॉन दूसरे स्थान पर जाते हैं जहाँ H+ आयन तथा घुली हुई ऑक्सीजन इन इलेक्ट्रॉनों को ग्रहण करती है। ये स्थान कैथोड की भाँति कार्य करते हैं।
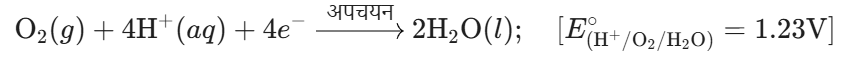
(iv) सम्पूर्ण अभिक्रिया अर्थात् अपचयोपचयन अभिक्रिया निम्न होती है।
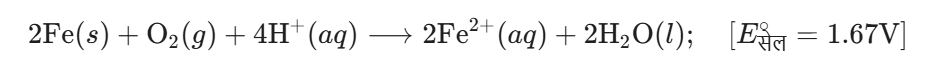
(v) फेरस आयन वायुमण्डलीय ऑक्सीजन द्वारा पुनः ऑक्सीकृत होकर फेरिक आयन बनाते हैं जो जल के अणुओं के साथ संयुक्त होकर जलीय फेरिक ऑक्साइड बनाते हैं।
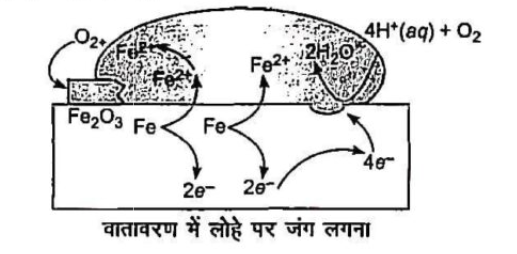
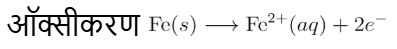
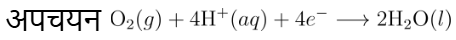
वायुमण्डलीय ऑक्सीकरण
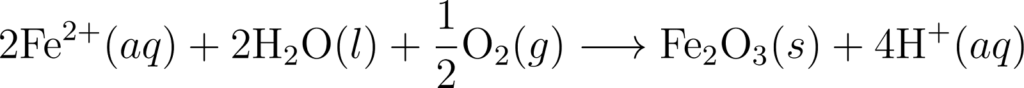
Q: नीचे दिए गए मानक इलेक्ट्रोड विभवों के आधार पर धातुओं को उनकी बढ़ती हुई अपचायक क्षमता के क्रम में व्यवस्थित कीजिए।
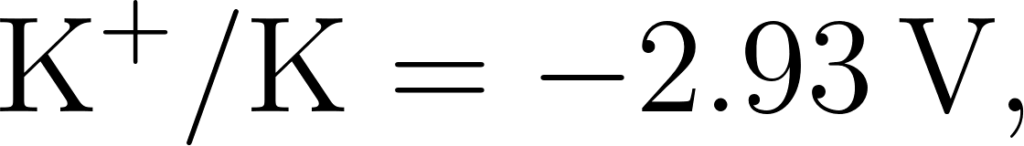
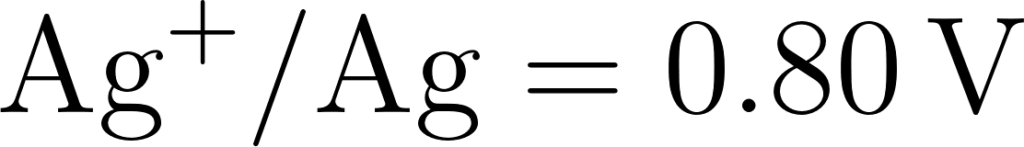
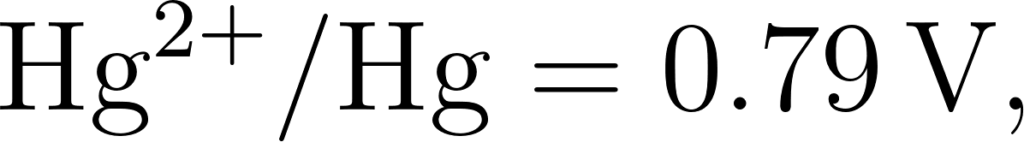
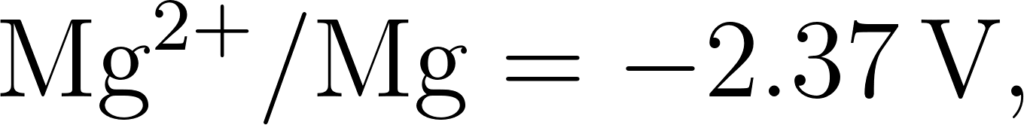
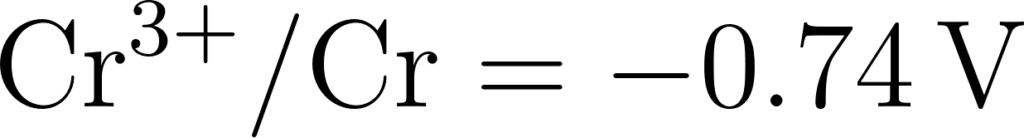
उत्तर: जिन धातुओं का अपचयन विभव निम्न (अधिक ऋणात्मक E0 मान) होता है। उनकी अपचायक क्षमता उतनी ही अधिक होती है क्योंकि ये स्वयं ही अधिक सरलता से ऑक्सीकृत हो जाते हैं।
