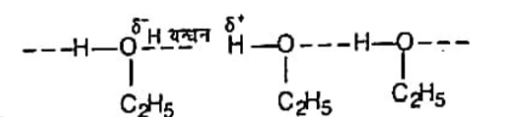इस पोस्ट मे हमने एनसीईआरटी के नवीनतम पाठ्यक्रम के अनुसार कक्षा 12 रसायनशास्त्र अध्याय 7 ऐल्कोहॉल, फीनॉल व ईथर का समाधान दिया हैं। हमने अध्याय मे मौजूद सभी प्रश्नों का समाधान सरल एवं स्पष्ट भाषा मे दिया हैं।
छात्रो के लिय ऐल्कोहॉल, फीनॉल व ईथर अध्याय को अच्छे से समझना बहुत जरूरी हैं। इस अध्याय की मदद से आईयूपीएसी (IUPAC) नामकरण, भौतिक गुण (हाइड्रोजन बंध), अल्कोहल का निर्जलीकरण, विलियमसन संश्लेषण, फीनॉल की अम्लता और इलेक्ट्रोफिलिक प्रतिस्थापन स्तर जैसी मूलभूत धारणाओ को अच्छे से समझ सकते हैं। परीक्षा मे अच्छा स्कोर करने के लिय इन धारणाओ को अच्छे से समझना बहुत जरूरी हैं।
ऐल्कोहॉल, फीनॉल व ईथर समाधान









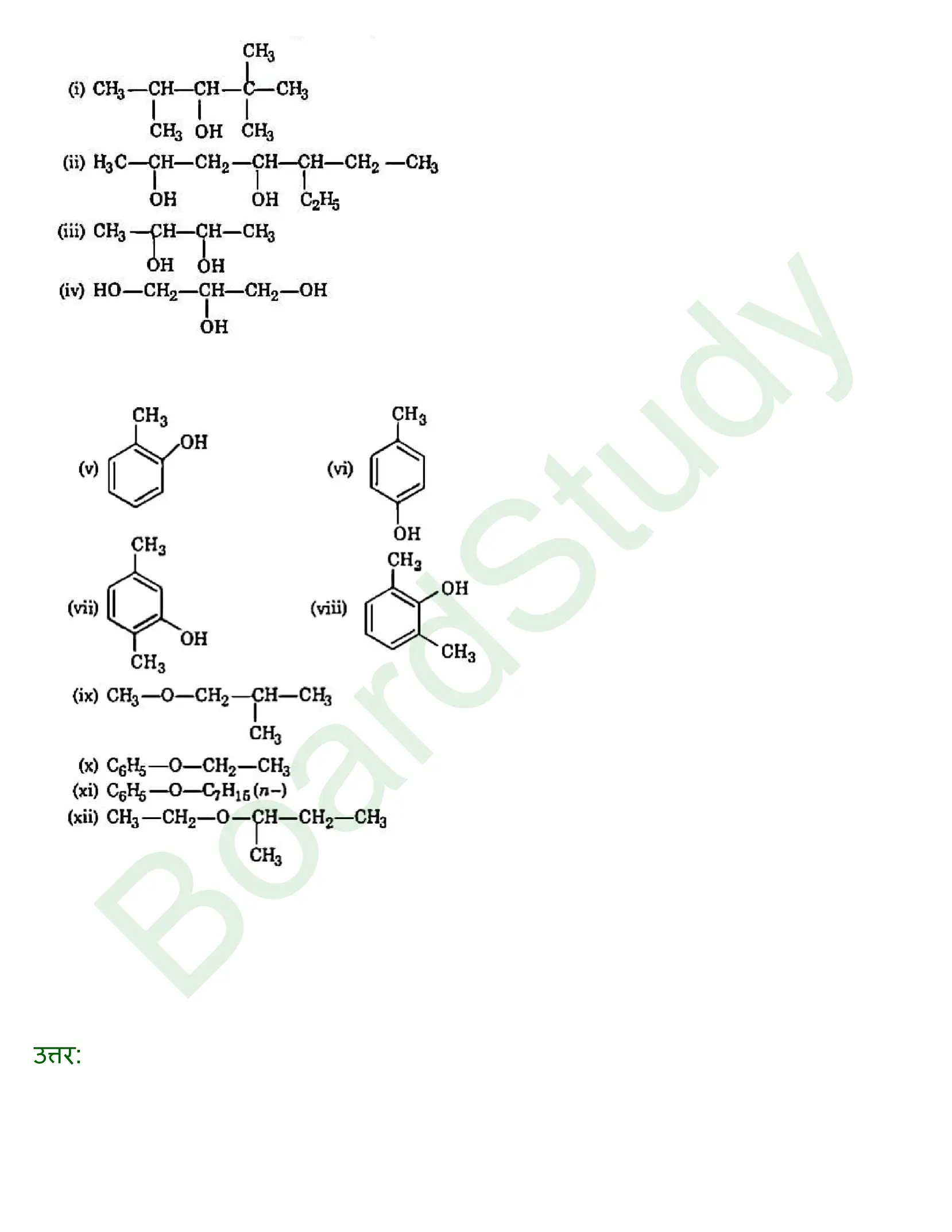

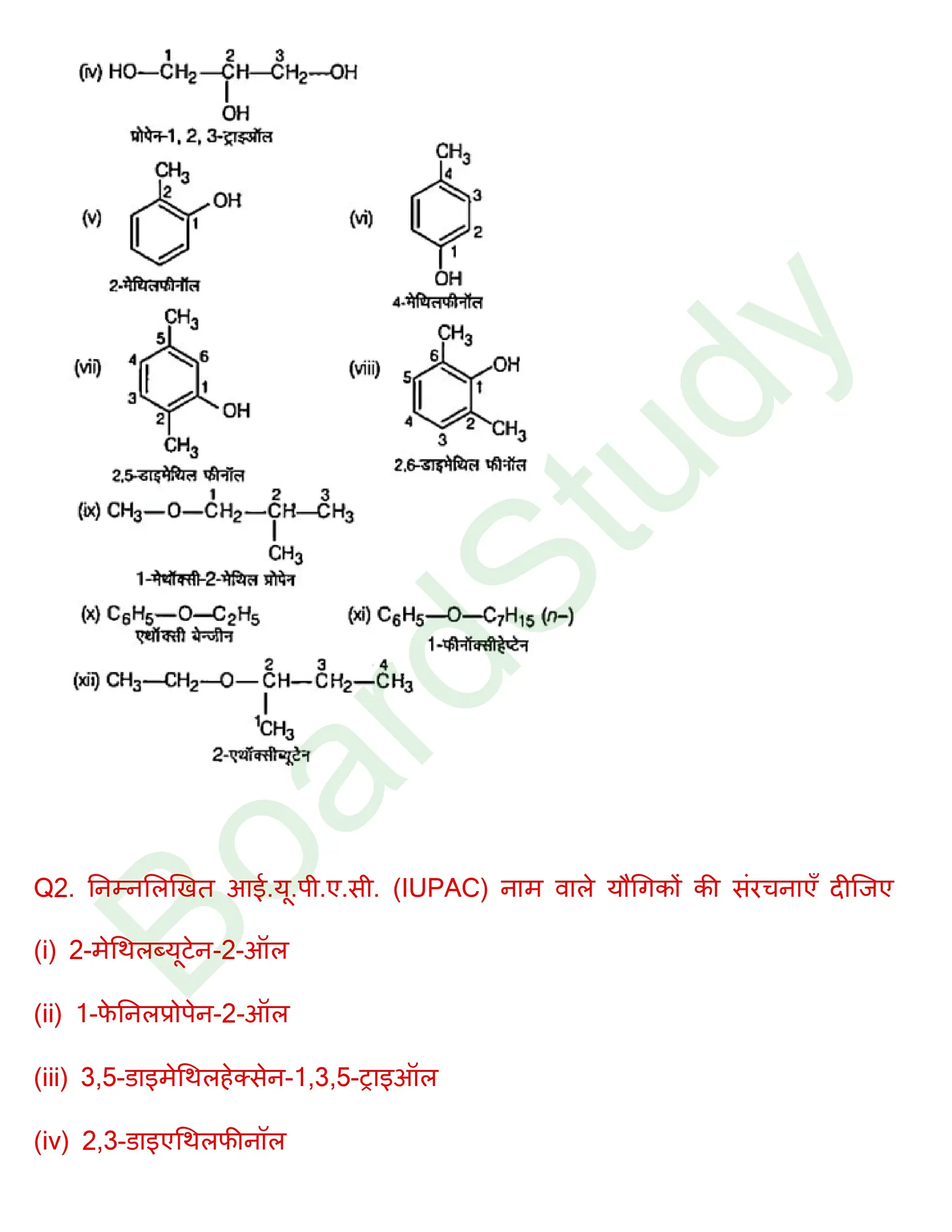
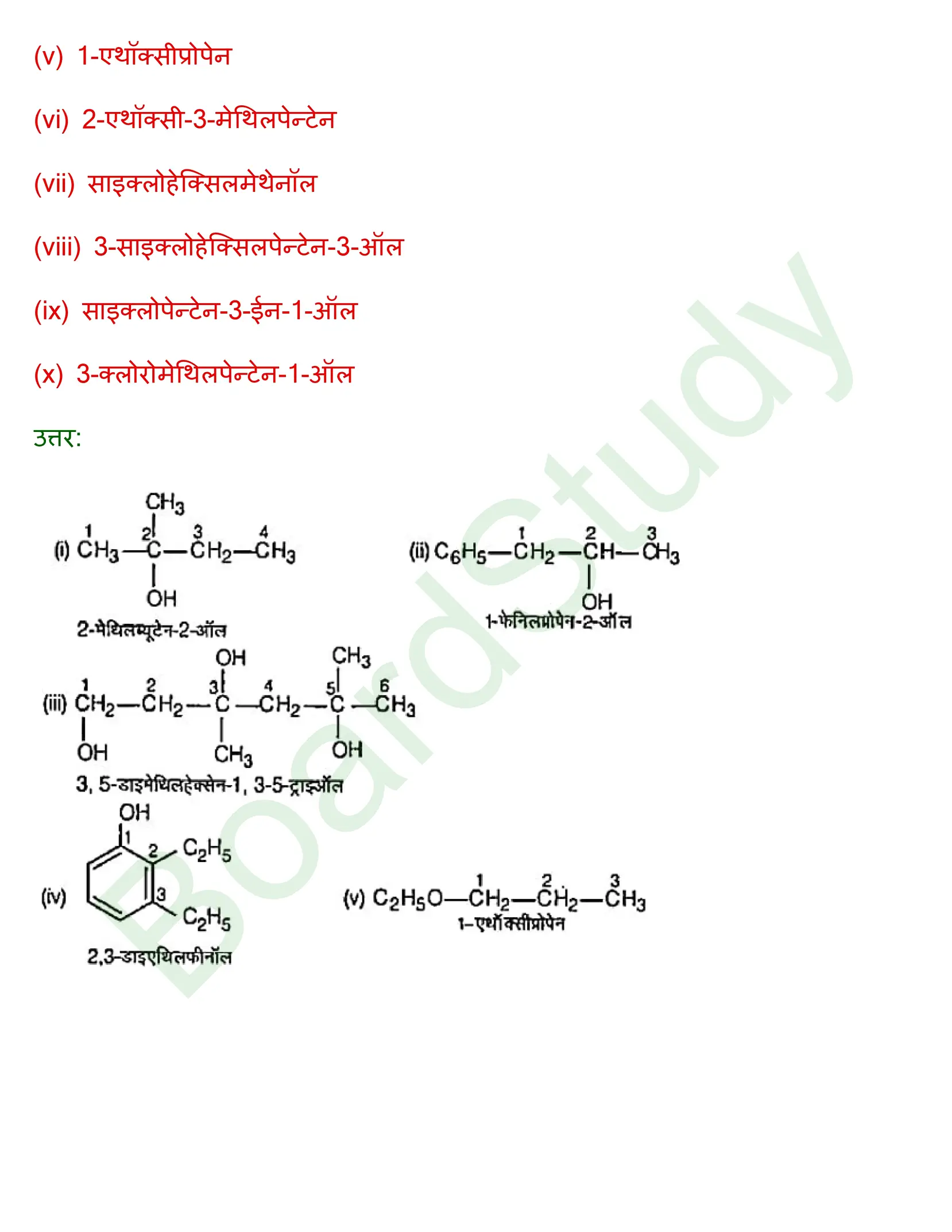
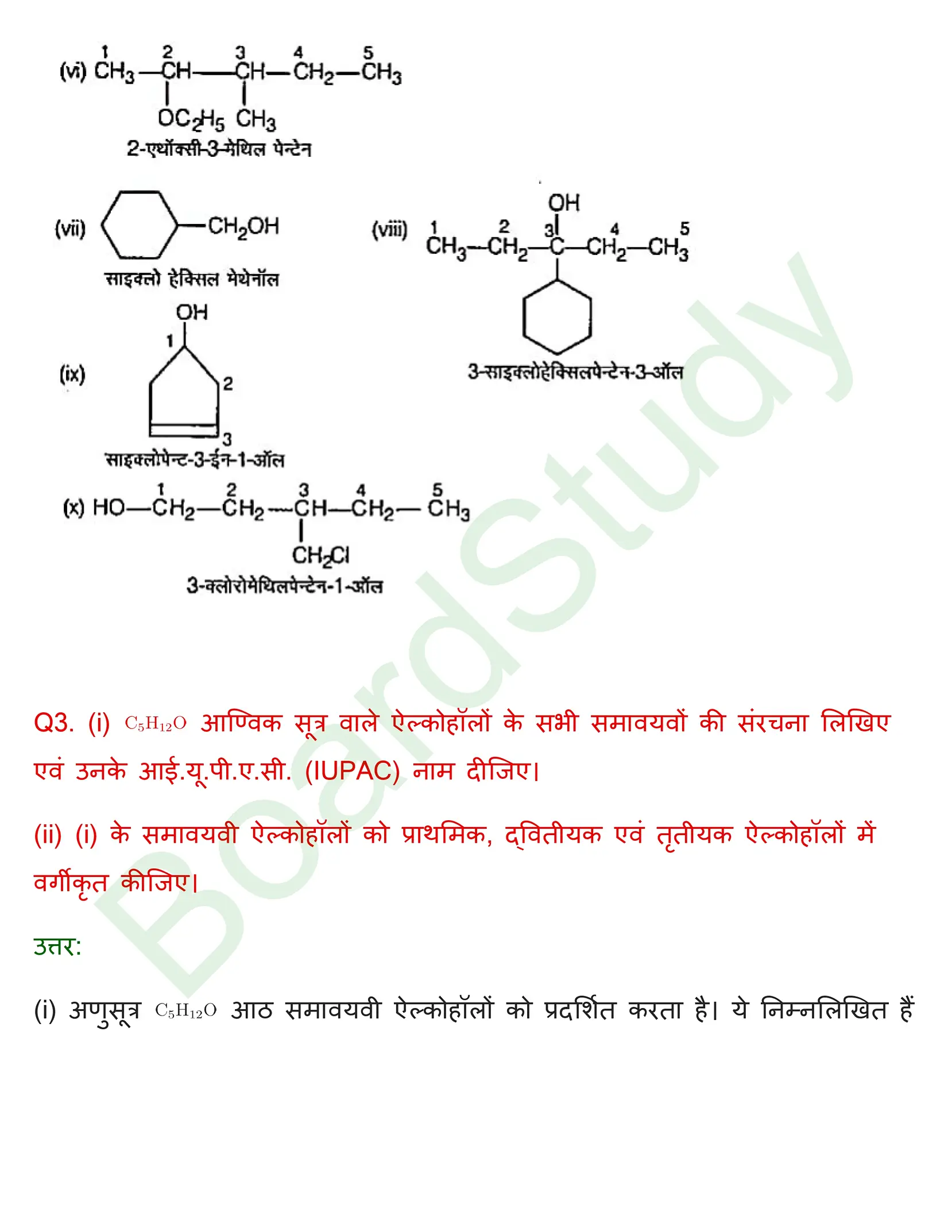








अध्याय 6: हैलोएल्केन और हैलोएरीन
अध्याय 8: ऐल्डिहाइड, किटोन एवं कार्बोक्सेिलिक अम्ल समाधान
अध्याय को अच्छे से समझने के लिय अध्याय मे दिय गय सभी प्रश्नों एवं अतिरिक्त प्रश्नों का अभ्यास बहुत जरूरी हैं। पिछले वर्ष का प्रश्न पत्र हल करना भी एक्जाम की तैयारी मे काफी मददगार साबित होता हैं।
एनसीईआरटी कक्षा 12 रसायनशास्त्र अध्याय 7 ऐल्कोहॉल, फीनॉल व ईथर के महत्वपूर्ण प्रश्न
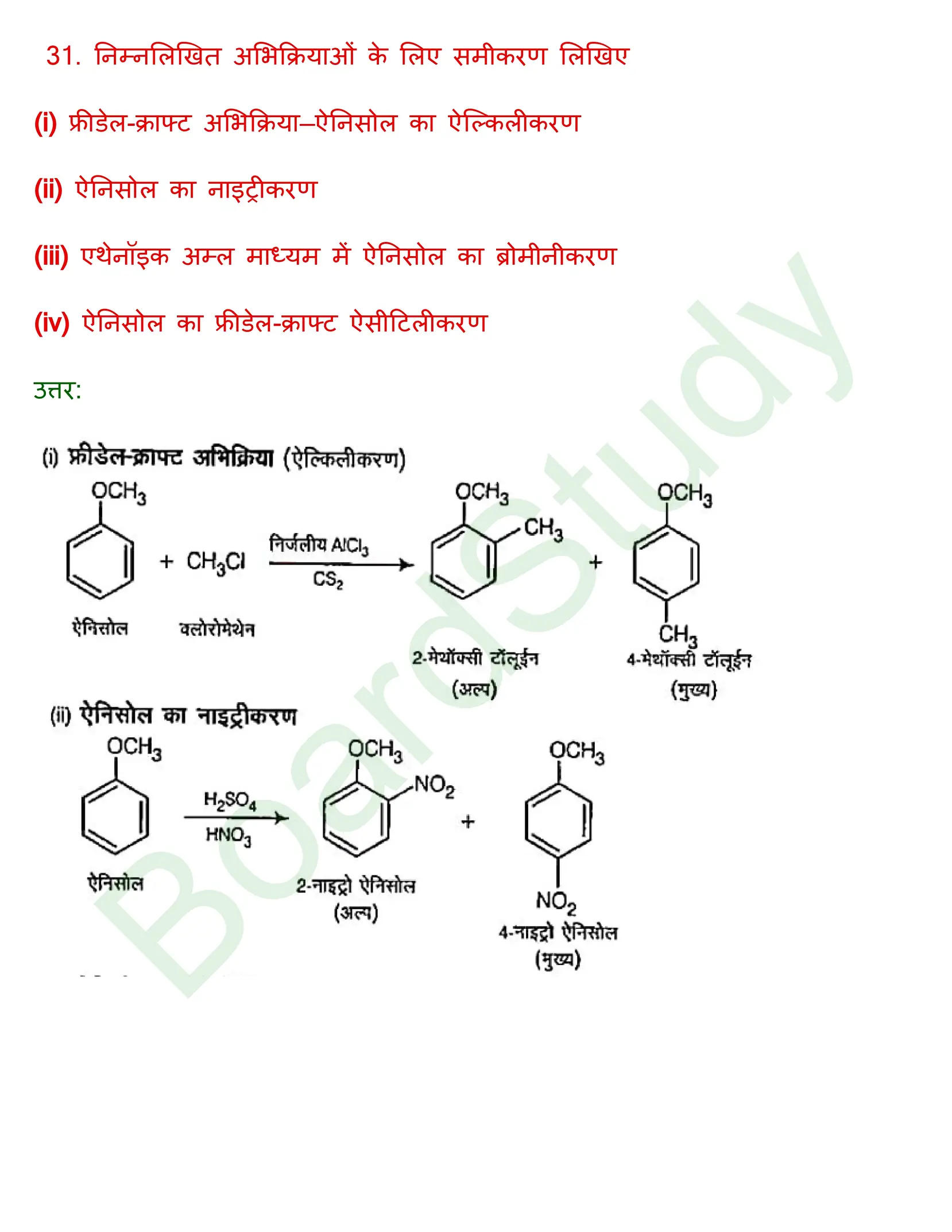
Q.निम्नलिखित को उदाहरण सहित समझाइए
(i) कोल्बे अभिक्रिया
(ii) राइमर-टीमन अभिक्रिया
(iii) विलियमसन ईथर संश्लेषण
(iv) असममित ईथर
उत्तर:
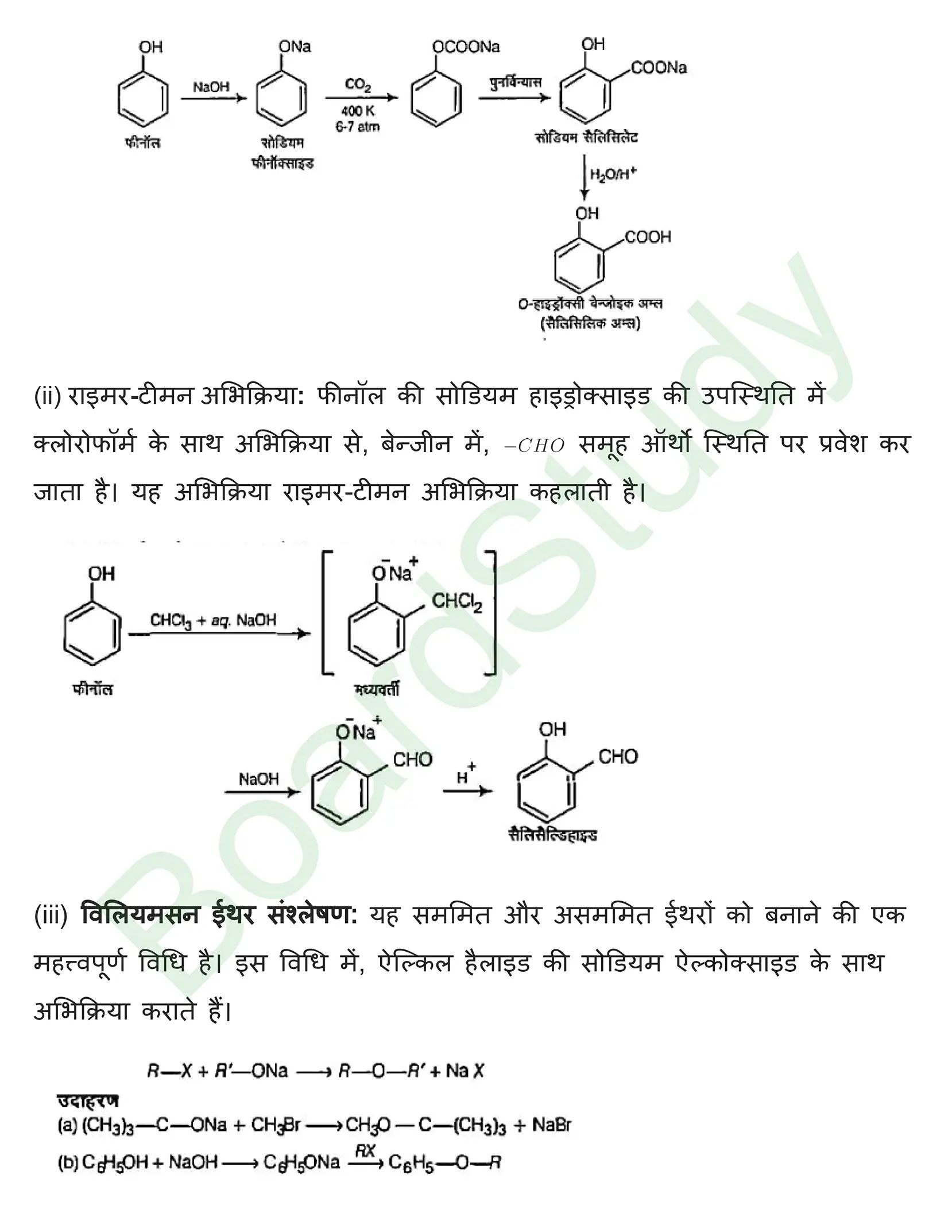
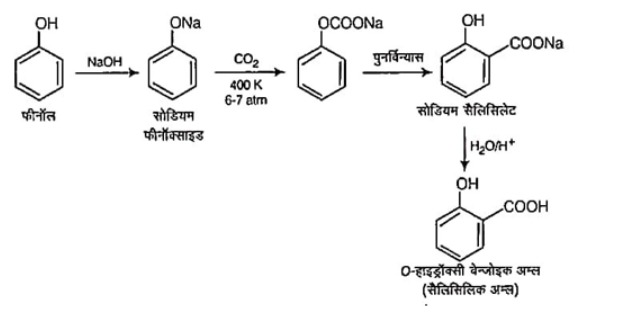
(i) कोल्बे अभिक्रिया: फीनॉल के सोडियम लवण अर्थात् सोडियम फीनॉक्सॉइड को लगभग 400K ताप तथा 4-7 वायुमण्डल दाब पर CO2 के साथ गर्म करने पर ऑर्थो स्थान पर -COOH समूह का प्रवेश होता है तथा मुख्य उत्पाद के रूप में सोडियम सैलिसिलेट प्राप्त होता है जो अम्लीकृत करने पर ऑर्थो हाइड्रॉक्सी बेन्जोइक अम्ल (सैलिसिलिक अम्ल) देता है। यह कोल्बे अभिक्रिया कहलाती है।
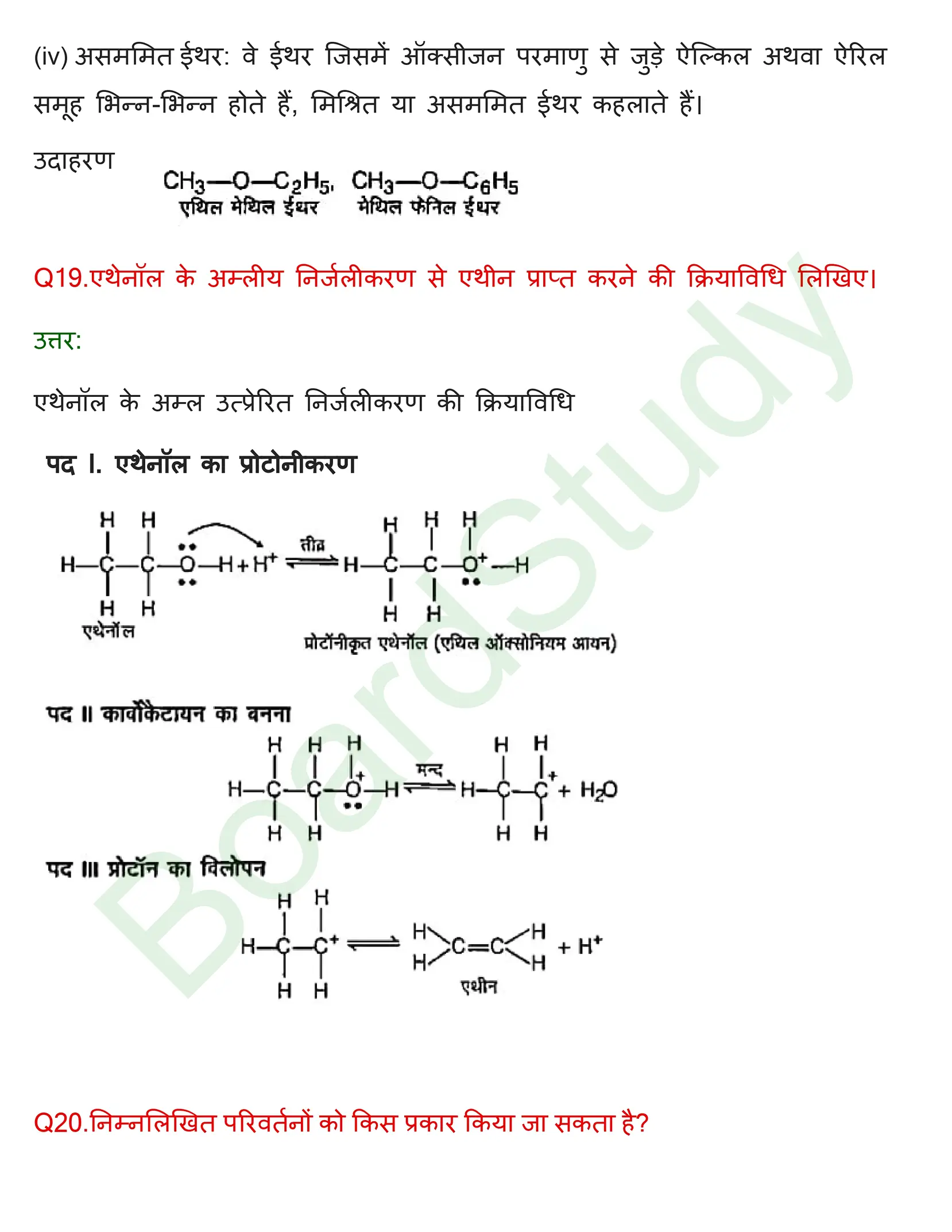
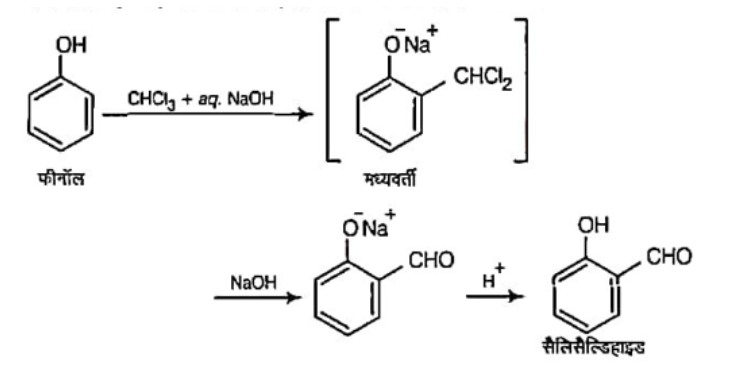
(ii) राइमर-टीमन अभिक्रिया: फीनॉल की सोडियम हाइड्रोक्साइड की उपस्थिति में क्लोरोफॉर्म के साथ अभिक्रिया से, बेन्जीन में, -CHO समूह ऑर्थो स्थिति पर प्रवेश कर जाता है। यह अभिक्रिया राइमर-टीमन अभिक्रिया कहलाती है।
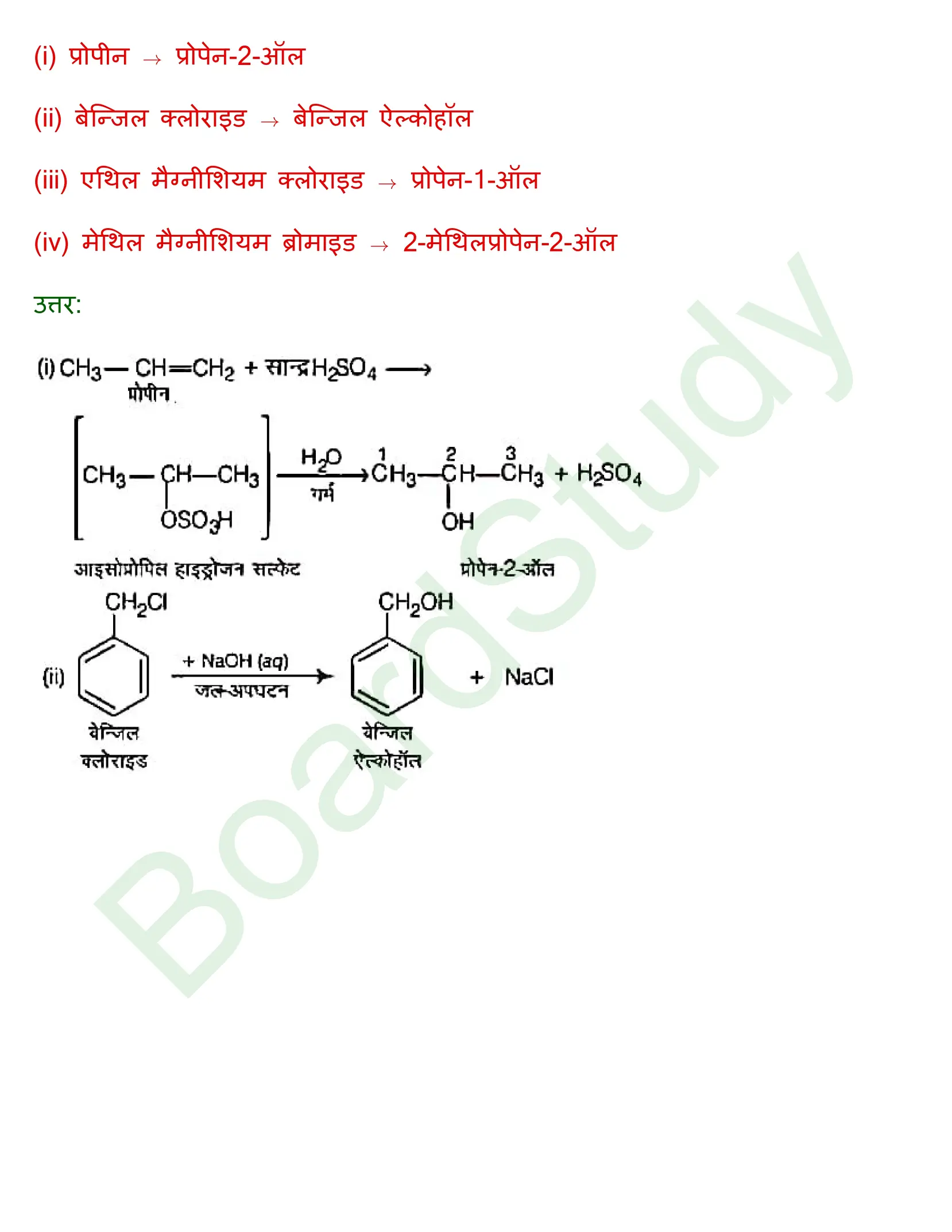
(iii) विलियमसन ईथर संश्लेषण: यह सममित और असममित ईथरों को बनाने की एक महत्त्वपूर्ण विधि है। इस विधि में, ऐल्किल हैलाइड की सोडियम ऐल्कोक्साइड के साथ अभिक्रिया कराते हैं।
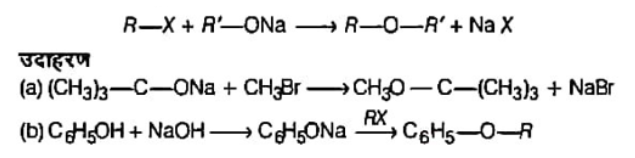
(iv) असममित ईथर: वे ईथर जिसमें ऑक्सीजन परमाणु से जुड़े ऐल्किल अथवा ऐरिल समूह भिन्न-भिन्न होते हैं, मिश्रित या असममित ईथर कहलाते हैं।
उदाहरण

Q. कारण बताइए कि मेथॉक्सिमेथेन की तुलना में एथेनॉल का क्वथनांक उच्च क्यों होता है?
उत्तर:
एथेनॉल अणुओं के मध्य हाइड्रोजन बन्धन उपस्थित होता है किन्तु यह मेथॉक्सिमेथेन के अणुओं में अनुपस्थित होता है। अतः एथेनॉल में अणुओं के हाइड्रोजन बन्धों से जुड़ा होने के कारण उन्हें अलग-अलग करने के लिए अधिक ऊर्जा की आवश्यकता होती है। इस कारण एथेनॉल का क्वथनांक मेथॉक्सिमेथेन की तुलना में अधिक होता है।